Lors de la réaction PCR, certains facteurs interférents sont souvent rencontrés.
En raison de la très grande sensibilité de la PCR, la contamination est considérée comme l'un des facteurs les plus importants affectant les résultats de la PCR et peut produire des résultats faussement positifs.
Les différentes sources de faux négatifs sont tout aussi cruciales. Si un ou plusieurs éléments essentiels du mélange PCR ou de la réaction d'amplification elle-même sont inhibés ou perturbés, le test diagnostique peut être compromis. Cela peut entraîner une baisse d'efficacité, voire des faux négatifs.
Outre l'inhibition, une perte d'intégrité des acides nucléiques cibles peut survenir en raison des conditions de transport et/ou de stockage avant la préparation des échantillons. En particulier, des températures élevées ou un stockage inadéquat peuvent endommager les cellules et les acides nucléiques. La fixation des cellules et des tissus ainsi que l'inclusion en paraffine sont des causes bien connues de fragmentation de l'ADN et constituent un problème persistant (voir figures 1 et 2). Dans ces cas, même une isolation et une purification optimales s'avèrent inefficaces.
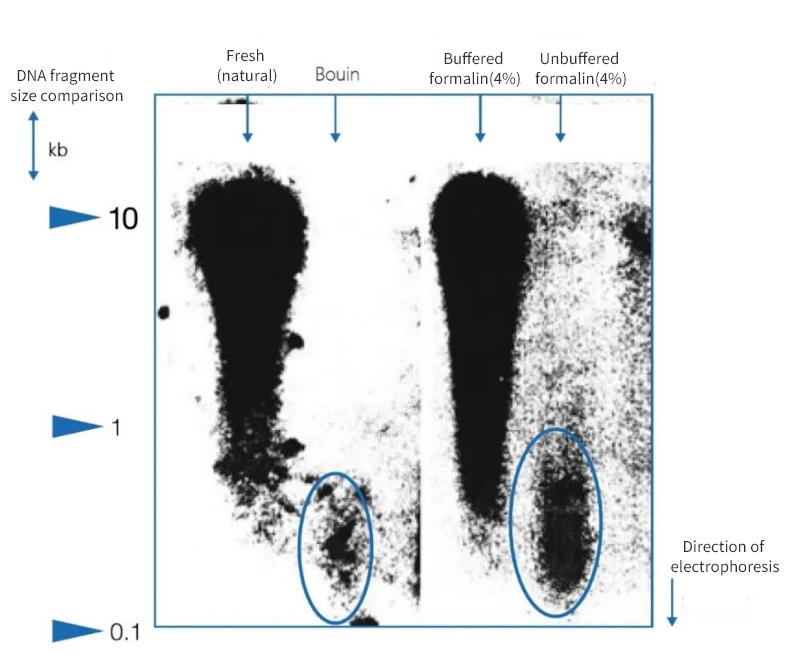
Figure 1 | Effet de l'immobilisation sur l'intégrité de l'ADN
L'électrophorèse sur gel d'agarose a révélé une grande variabilité de la qualité de l'ADN extrait de coupes de paraffine issues d'autopsies. La longueur moyenne des fragments d'ADN variait considérablement selon la méthode de fixation. L'ADN était préservé uniquement lors de la fixation sur des échantillons congelés natifs et dans du formol neutre tamponné. L'utilisation d'un fixateur de Bouin fortement acide ou de formol non tamponné contenant de l'acide formique entraînait une perte significative d'ADN. La fraction restante est fortement fragmentée.
À gauche, la longueur des fragments est exprimée en kilobases (kbp).
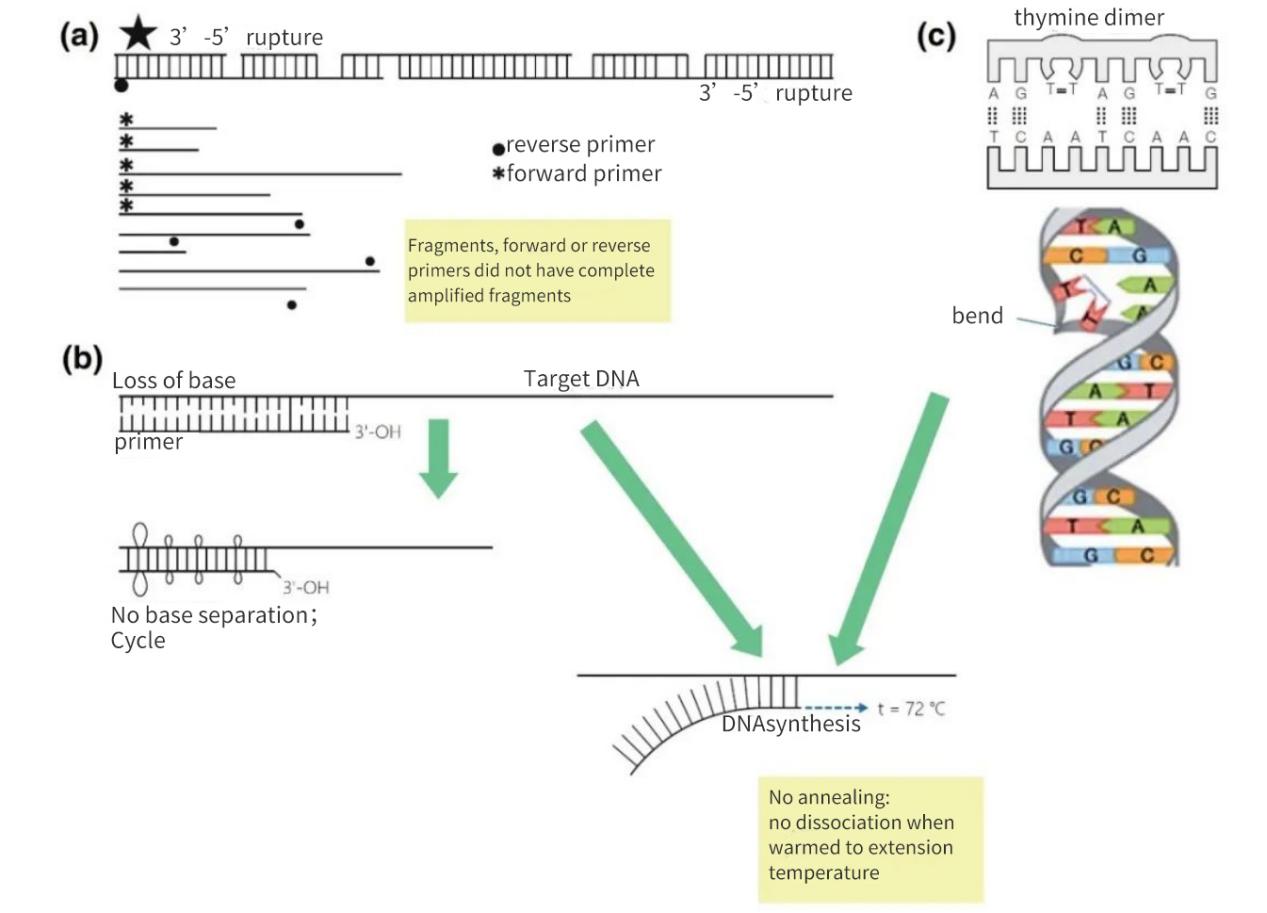
Figure 2 | Perte d'intégrité des cibles d'acides nucléiques
(a) Un espace 3′-5′ sur les deux brins entraîne une coupure dans l’ADN cible. La synthèse d’ADN se poursuit sur le petit fragment. Cependant, si un site d’hybridation d’amorce est absent sur le fragment d’ADN, seule une amplification linéaire a lieu. Dans le meilleur des cas, les fragments peuvent se resaturer, mais les rendements seront faibles et inférieurs au seuil de détection.
(b) La perte de bases, principalement due à la dépurination et à la formation de dimères de thymidine, entraîne une diminution du nombre de liaisons hydrogène et une diminution de la température de fusion (Tm). Au cours de la phase de réchauffement prolongée, les amorces se détachent de l'ADN matrice et ne s'hybrident pas, même dans des conditions moins strictes.
(c) Les bases thymine adjacentes forment un dimère TT.
Un autre problème fréquent en diagnostic moléculaire est la libération sous-optimale des acides nucléiques cibles par rapport à l'extraction au phénol-chloroforme. Dans les cas extrêmes, cela peut entraîner des faux négatifs. Le lyse par ébullition ou la digestion enzymatique des débris cellulaires permettent un gain de temps considérable, mais cette méthode conduit souvent à une faible sensibilité de la PCR en raison d'une libération insuffisante d'acides nucléiques.
Inhibition de l'activité de la polymérase pendant l'amplification
De manière générale, le terme « inhibition » englobe tous les facteurs qui conduisent à des résultats de PCR sous-optimaux. Au sens strictement biochimique, l’inhibition se limite à l’activité enzymatique ; autrement dit, elle réduit ou empêche la conversion du substrat en produit par interaction avec le site actif de l’ADN polymérase ou son cofacteur (par exemple, Mg²⁺ pour la Taq polymérase).
Les composants de l'échantillon ou divers tampons et extraits contenant des réactifs peuvent inhiber directement l'enzyme ou piéger ses cofacteurs (par exemple l'EDTA), inactivant ainsi la polymérase et conduisant à des résultats PCR diminués ou faussement négatifs.
Cependant, de nombreuses interactions entre les composants de la réaction et les acides nucléiques contenant la cible sont également qualifiées d’« inhibiteurs de PCR ». Une fois l’intégrité cellulaire compromise par l’isolement et l’acide nucléique libéré, des interactions peuvent se produire entre l’échantillon et son milieu environnant (solution et phase solide). Par exemple, des « séquestrants » peuvent se lier à l’ADN simple ou double brin par des interactions non covalentes et interférer avec l’isolement et la purification en réduisant le nombre de cibles atteignant finalement le réacteur de PCR.
En général, les inhibiteurs de la PCR sont présents dans la plupart des fluides corporels et des réactifs utilisés pour les tests de diagnostic clinique (urée dans l'urine, hémoglobine et héparine dans le sang), les compléments alimentaires (composants organiques, glycogène, graisses, ions Ca2+) et les composants de l'environnement (phénols, métaux lourds).
| Inhibiteurs | Source |
| ions calcium | Lait, tissu osseux |
| collagène | Tissu |
| sels biliaires | matières fécales |
| Hémoglobine | Dans le sang |
| Hémoglobine | échantillons de sang |
| Acide humique | sol, plante |
| Sang | Sang |
| Lactoferrine | Sang |
| (européenne) mélanine | peau, cheveux |
| Myoglobine | Tissu musculaire |
| Polysaccharides | Plante, excréments |
| Protéase | Lait |
| Urée | Urine |
| mucopolysaccharide | Cartilage, muqueuses |
| Lignine, cellulose | Plantes |
Les inhibiteurs de PCR les plus fréquents se trouvent dans les bactéries et les cellules eucaryotes, l'ADN non ciblé, les macromolécules se liant à l'ADN présentes dans les matrices tissulaires et le matériel de laboratoire comme les gants et les plastiques. La purification des acides nucléiques pendant ou après l'extraction est la méthode privilégiée pour éliminer ces inhibiteurs.
Aujourd'hui, divers équipements d'extraction automatisés peuvent remplacer de nombreux protocoles manuels, mais la récupération et/ou la purification à 100 % des cibles n'ont jamais été atteintes. Des inhibiteurs potentiels peuvent encore être présents dans les acides nucléiques purifiés ou avoir déjà agi. Différentes stratégies existent pour réduire l'impact des inhibiteurs. Le choix de la polymérase appropriée peut avoir un impact significatif sur l'activité inhibitrice. D'autres méthodes éprouvées pour réduire l'inhibition de la PCR consistent à augmenter la concentration de la polymérase ou à utiliser des additifs tels que la BSA.
L'inhibition des réactions PCR peut être démontrée par l'utilisation d'un contrôle de qualité interne (IPC).
Il est impératif d'éliminer soigneusement, par un lavage complet, tous les réactifs et autres solutions présents dans le kit d'extraction, tels que l'éthanol, l'EDTA, le CETAB, le LiCl, le GuSCN, le SDS, l'isopropanol et le phénol, de l'isolat d'acide nucléique. Selon leur concentration, ces réactifs peuvent activer ou inhiber la PCR.
Date de publication : 19 mai 2023
 中文网站
中文网站