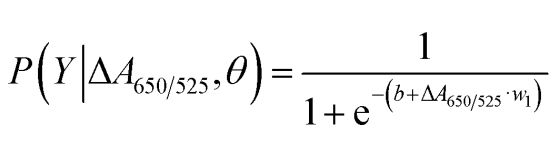Le dépistage précoce du cancer par biopsie liquide est une nouvelle approche de détection et de diagnostic du cancer proposée ces dernières années par l'Institut national du cancer américain, dans le but de détecter les cancers à un stade précoce, voire les lésions précancéreuses. Cette technique est largement utilisée comme nouveau biomarqueur pour le diagnostic précoce de diverses tumeurs malignes, notamment le cancer du poumon, les tumeurs gastro-intestinales, les gliomes et les tumeurs gynécologiques.
L'émergence de plateformes permettant d'identifier les biomarqueurs du paysage de méthylation (Methylscape) pourrait améliorer considérablement le dépistage précoce du cancer, permettant ainsi de prendre en charge les patients au stade le plus précoce et traitable.
Des chercheurs ont récemment mis au point une plateforme de détection simple et directe du profil de méthylation, basée sur des nanoparticules d'or fonctionnalisées à la cystéamine (Cyst/AuNPs) et un biocapteur pour smartphone. Cette plateforme permet un dépistage précoce et rapide d'un large éventail de tumeurs. Le dépistage précoce de la leucémie peut être réalisé dans les 15 minutes suivant l'extraction d'ADN à partir d'un échantillon sanguin, avec une précision de 90 %. L'article s'intitule : « Détection rapide de l'ADN cancéreux dans le sang humain à l'aide de nanoparticules d'or fonctionnalisées à la cystéamine et d'un smartphone doté d'un système d'apprentissage automatique ».
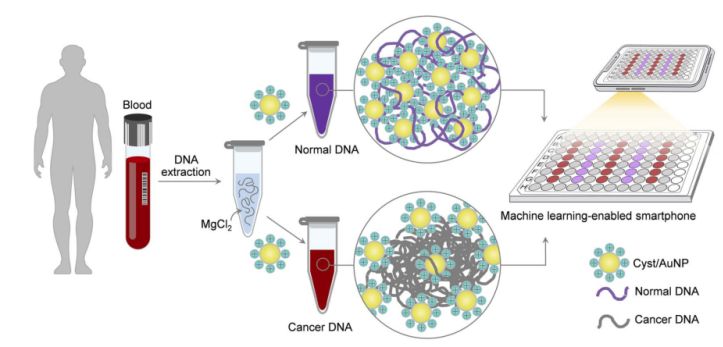
Figure 1. Une plateforme de détection simple et rapide pour le dépistage du cancer via des composants Cyst/AuNPs peut être réalisée en deux étapes simples.
Ceci est illustré sur la figure 1. Dans un premier temps, une solution aqueuse a été utilisée pour dissoudre les fragments d'ADN. Des nanoparticules d'or (Cyst/AuNPs) ont ensuite été ajoutées à la solution obtenue. L'ADN normal et l'ADN malin présentent des propriétés de méthylation différentes, ce qui engendre des fragments d'ADN aux profils d'auto-assemblage distincts. L'ADN normal s'agrège de manière lâche et finit par agréger les Cyst/AuNPs, ce qui explique le décalage spectral vers le rouge de ces dernières, permettant ainsi d'observer à l'œil nu un changement de couleur du rouge au violet. En revanche, le profil de méthylation spécifique de l'ADN cancéreux conduit à la formation d'agrégats plus importants de fragments d'ADN.
Des images de plaques à 96 puits ont été prises à l'aide d'un smartphone. L'ADN cancéreux a été mesuré par un smartphone équipé d'un système d'apprentissage automatique, et comparé aux méthodes spectroscopiques.
Dépistage du cancer dans de véritables échantillons de sang
Pour étendre les possibilités de la plateforme de détection, les chercheurs ont utilisé un capteur capable de distinguer l'ADN normal de l'ADN cancéreux dans de véritables échantillons de sang. Les profils de méthylation des sites CpG régulent épigénétiquement l'expression des gènes. Dans la quasi-totalité des types de cancer, on observe une alternance des modifications de la méthylation de l'ADN et, par conséquent, de l'expression des gènes favorisant la tumorigénèse.
Afin d'étudier l'efficacité du profil de méthylation pour différencier les cancers leucémiques, les chercheurs ont utilisé des échantillons sanguins de patients atteints de leucémie et de témoins sains comme modèle pour d'autres cancers associés à la méthylation de l'ADN. Ce biomarqueur de profil de méthylation surpasse non seulement les méthodes de dépistage rapide de la leucémie existantes, mais démontre également la faisabilité de son application au dépistage précoce d'un large éventail de cancers grâce à ce test simple et direct.
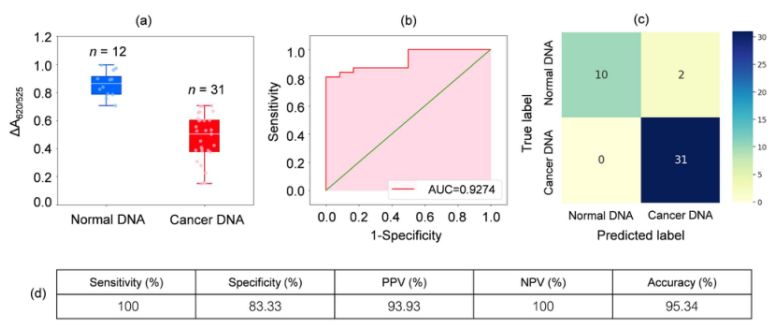
L'ADN extrait d'échantillons sanguins de 31 patients atteints de leucémie et de 12 individus sains a été analysé. Comme illustré par le diagramme en boîte de la figure 2a, l'absorbance relative des échantillons cancéreux (ΔA650/525) était inférieure à celle de l'ADN des échantillons normaux. Ceci était principalement dû à l'hydrophobicité accrue induisant une forte agrégation de l'ADN cancéreux, empêchant ainsi l'agrégation des Cyst/AuNPs. Par conséquent, ces nanoparticules étaient complètement dispersées dans les couches externes des agrégats cancéreux, ce qui entraînait une dispersion différente des Cyst/AuNPs adsorbées sur les agrégats d'ADN normal et cancéreux. Des courbes ROC ont ensuite été générées en faisant varier le seuil de ΔA650/525, d'une valeur minimale à une valeur maximale.
Figure 2.(a) Valeurs d'absorbance relative des solutions de kystes/AuNPs montrant la présence d'ADN normal (bleu) et cancéreux (rouge) dans des conditions optimisées
(DA650/525) des diagrammes en boîte ; (b) Analyse ROC et évaluation des tests diagnostiques. (c) Matrice de confusion pour le diagnostic des patients sains et cancéreux. (d) Sensibilité, spécificité, valeur prédictive positive (VPP), valeur prédictive négative (VPN) et exactitude de la méthode développée.
Comme illustré sur la figure 2b, l'aire sous la courbe ROC (AUC = 0,9274) obtenue pour le capteur développé a démontré une sensibilité et une spécificité élevées. Le diagramme en boîte montre que le point le plus bas, représentant le groupe d'ADN normal, n'est pas nettement distinct du point le plus haut, représentant le groupe d'ADN cancéreux. Par conséquent, une régression logistique a été utilisée pour différencier les groupes normal et cancéreux. Ce modèle, étant donné un ensemble de variables indépendantes, estime la probabilité d'occurrence d'un événement, tel que l'appartenance au groupe normal ou cancéreux. La variable dépendante varie entre 0 et 1. Le résultat est donc une probabilité. Nous avons déterminé la probabilité d'identification d'un cancer (P) à partir du rapport ΔA650/525 comme suit.
où b = 5,3533 et w1 = -6,965. Pour la classification des échantillons, une probabilité inférieure à 0,5 indique un échantillon normal, tandis qu'une probabilité supérieure ou égale à 0,5 indique un échantillon cancéreux. La figure 2c présente la matrice de confusion générée par validation croisée « leave-it-alone », utilisée pour valider la stabilité de la méthode de classification. La figure 2d résume l'évaluation diagnostique de la méthode, incluant la sensibilité, la spécificité, la valeur prédictive positive (VPP) et la valeur prédictive négative (VPN).
biocapteurs basés sur les smartphones
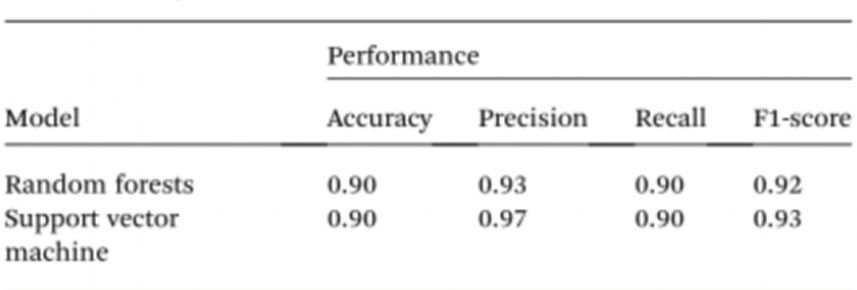
Afin de simplifier davantage l'analyse des échantillons sans recourir à des spectrophotomètres, les chercheurs ont utilisé l'intelligence artificielle (IA) pour interpréter la couleur de la solution et distinguer les échantillons sains des échantillons cancéreux. Ainsi, la vision par ordinateur a permis de traduire la couleur de la solution de kystes/nanoparticules d'or (Kyst/AuNPs) en ADN normal (violet) ou ADN cancéreux (rouge) à partir d'images de plaques 96 puits prises avec un smartphone. L'intelligence artificielle peut réduire les coûts et améliorer l'accessibilité de l'interprétation de la couleur des solutions de nanoparticules, et ce, sans nécessiter d'accessoires optiques pour smartphone. Enfin, deux modèles d'apprentissage automatique, Random Forest (RF) et Support Vector Machine (SVM), ont été entraînés pour construire les modèles. Les deux modèles (RF et SVM) ont classé correctement les échantillons comme positifs ou négatifs avec une précision de 90 %. Ceci suggère que l'utilisation de l'intelligence artificielle dans la biodétection mobile est tout à fait envisageable.
Figure 3. (a) Classe cible de la solution enregistrée lors de la préparation de l'échantillon pour l'acquisition d'images. (b) Exemple d'image prise lors de l'acquisition d'images. (c) Intensité de couleur de la solution kyste/AuNPs dans chaque puits de la plaque 96 puits, extraite de l'image (b).
Grâce à la technologie Cyst/AuNPs, des chercheurs ont mis au point une plateforme de détection simple pour l'analyse du profil de méthylation et un capteur capable de distinguer l'ADN normal de l'ADN cancéreux à partir d'échantillons de sang réels utilisés pour le dépistage de la leucémie. Ce capteur a permis de détecter rapidement et à moindre coût de faibles quantités d'ADN cancéreux (3 nM) chez des patients atteints de leucémie en seulement 15 minutes, avec une précision de 95,3 %. Afin de simplifier davantage l'analyse des échantillons en s'affranchissant du spectrophotomètre, l'apprentissage automatique a été utilisé pour interpréter la couleur de la solution et différencier les individus sains des individus cancéreux à partir d'une photographie prise avec un téléphone portable. Une précision de 90,0 % a ainsi été obtenue.
Référence : DOI : 10.1039/d2ra05725e
Date de publication : 18 février 2023
 中文网站
中文网站